Hãy trình bày tính chất hóa học của axit sunfuric\, với mỗi tính chất chất hóa học hãy dẫn ra một PTHH để minh họa.

Những câu hỏi liên quan
hãy chỉ ra những tính chất hóa học chung và khác biệt giữa axit nitric và axit sunfuric . hãy viết phương trình hóa học để minh họa .
Axit nitric và axit sunfuric đặc đều có tính oxi hóa mạnh.
Ví dụ: 3FeO +10HNO3 —> 3Fe(NO3)3 + NO ↓+ 5H2O
2FeO + 4H2SO4 —> Fe2SO4)3 + SO2 + 4H2O
Tuy nhiên nếu như HNO3 loãng vẫn có tính oxi hóa thì H2SO4 loãng lại không có tính oxi hóa. Ví dụ
3Fe3O4 + 28HNO3 l -> 9Fe(NO3)3 + NO↓+ 14H2O Fe3O4 + 4H2SO4 l —> FeSO4 + Fe2(S04)3 + 4H2O
Đúng 0
Bình luận (0)
Trong hợp nào axit sunfuric có nhưng tính chất hóa học chung của một axit ? Đó là những tính chất nào? Dẫn ra những phương trình phản ứng để minh họa.
Dung dịch axit sunfuric loãng có những tính chất chung của axit, đó là:
- Đổi màu quỳ tím thành đỏ.
- Tác dụng với kim loại giải phóng hiđro.
Fe + H2SO4 → FeSO4 + H2
- Tác dụng với oxit bazơ và bazơ
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
- Tính chất với nhiều chất muối
BaCl2 + H2SO4 → BaSO4 +2HCl
Đúng 0
Bình luận (0)
Khi khí H2S và axit H2SO4 tham gia các phản ứng oxi hóa – khử, người ta có nhận xét:
- Hidro sunfua chỉ thể hiện tính khử.
- Axit sunfuric chỉ thể hiện tính oxi hóa.
a) Hãy giải thích điều nhận xét trên.
b) Đối với mỗi chất, hãy dẫn ra một phản ứng hóa học để minh họa.
a) Khí H2S và axit sunfuric đặc tham gia các phản ứng oxi hóa – khử thì khí H2S chỉ thể hiện tính khử và H2SO4 đặc chỉ thể hiện tính oxi hóa. Vì trong H2S số oxi hóa của S chỉ có thể tăng, trong H2SO4 số oxi hóa S chỉ có thể giảm.
Vì trong H2S số oxi hóa của S là -2 (là số oxi hóa thấp nhất của S) nên chỉ có thể tăng (chỉ thể hiện tính khử), trong H2SO4 số oxi hóa của S là +6 (là số oxi hóa cao nhất của S) nên chỉ có thể giảm (chỉ thể hiện tính oxi hóa).
b) Phương trình phản ứng hóa học:
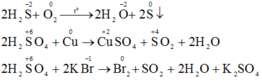
Đúng 0
Bình luận (0)
Trình bày tính chất hóa học của nước, mỗi tính chất viết 2 PTHH để minh họa
- Tác dụng với kim loại:
Nước có thể tác dụng với một số kim loại ở nhiệt độ thường như Ca, Ba, K,…
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
- Tác dụng với một số oxit bazo như CaO, K2O,… tạo ra bazo tương ứng Ca(OH)2, KOH,…
\(K_2O+H_2O\rightarrow2KOH\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
- Tác dụng với oxit axit như SO3, P2O5… tạo thành axit tương ứng H2SO4, H3PO4,…
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
Đúng 3
Bình luận (0)
Trong trường hợp nào axit sunfuric có những tính chất hóa học đặc trưng? Đó là những tính chất nào? Dẫn ra những phương trình phản ứng để minh họa.
Tính chất hóa học đặc trưng của axit sunfuric đặc là tính oxi hóa mạnh và tính háo nước.
- Tính chất oxi hóa mạnh
2H2SO4 + Cu → CuSO4 + SO2 + 2H2O
2H2SO4 + S → 3SO2 + 2H2O
2H2SO4 + 2KBr → Br2 + SO2 + 2H2O + K2SO4
- Tính háo nước và tính chất oxi hóa
Axit sunfuric đặc háp thụ mạnh nước. Axit sunfuric đặc chiếm các nguyên tử H và O là những nguyên tố thành phần của các hợp chất gluxit giải phóng cacbon và nước.
C12H22O11 → 12C + 11H2O.
Da thịt tiếp xúc với H2SO4 đặc sẽ bị bỏng rất nặng, vì vậy khi sử dụng axit sunfuric phải hết sức thận trọng.
Đúng 0
Bình luận (0)
1, hãy trình bày tính chất hóa học của oxit? mỗi tính chất lấy 3 vd? phân loại oxit?2, hãy trình bày tính chất hóa học của axit? mỗi tính chất lấy 3 vd? phân loại axit?3, hãy trình bày tính chất hóa học của bazơ? mỗi tính chất lấy 3 vd? phân loại bazơ?4,hãy trình bày tính chất hóa học của muối? mỗi tính chất lấy 3 vd? phân loại muối?5, hãy trình bày tính chất hóa học của sắt và nhôm? mỗi tính chất lấy 2 vd? chúng có phản ứng nào đặc trưng nhất? ptpư6,hãy trình bày tính chất hóa học chung của kim...
Đọc tiếp
1, hãy trình bày tính chất hóa học của oxit? mỗi tính chất lấy 3 vd? phân loại oxit?
2, hãy trình bày tính chất hóa học của axit? mỗi tính chất lấy 3 vd? phân loại axit?
3, hãy trình bày tính chất hóa học của bazơ? mỗi tính chất lấy 3 vd? phân loại bazơ?
4,hãy trình bày tính chất hóa học của muối? mỗi tính chất lấy 3 vd? phân loại muối?
5, hãy trình bày tính chất hóa học của sắt và nhôm? mỗi tính chất lấy 2 vd? chúng có phản ứng nào đặc trưng nhất? ptpư
6,hãy trình bày tính chất hóa học chung của kim loại và phi kim? mỗi tính chất lấy vd? tính chất hóa học đặc trưng của khí Cl2 và cacbon?
a)Trong các trường hợp nào của axit sunfuric có những tính chất hóa học chung của một axit ? Đó là những tính chất nào ? Dẫn ra phương trình phản ứng để minh họa.
b) Trong trường hợp nào axit sunfuric có những tính chất hóa học đặc trưng ?
Đó là những tính chất nào ? Dẫn ra phương trình phản ứng để minh họa.
Đọc tiếp
a)Trong các trường hợp nào của axit sunfuric có những tính chất hóa học chung của một axit ? Đó là những tính chất nào ? Dẫn ra phương trình phản ứng để minh họa.
b) Trong trường hợp nào axit sunfuric có những tính chất hóa học đặc trưng ?
Đó là những tính chất nào ? Dẫn ra phương trình phản ứng để minh họa.
a) Dung dịch axit sunfuric loãng có những tính chất chung của axit, đó là:
- Đổi màu quỳ tím thành đỏ.
- Tác dụng với kim loại giải phóng hiđro.
Fe + H2SO4 → FeSO4 + H2
- Tác dụng với oxit bazơ và bazơ
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
- Tính chất với nhiều chất muối
BaCl2 + H2SO4 → BaSO4 +2HCl
b) Tính chất hóa học đặc trưng của axit sunfuric đặc là tính oxi hóa mạnh và tính háo nước.
- Tính chất oxi hóa mạnh
2H2SO4 + Cu → CuSO4 + SO2 + 2H2O
2H2SO4 + S → 3SO2 + 2H2O
2H2SO4 + 2KBr → Br2 + SO2 + 2H2O + K2SO4
- Tính háo nước và tính chất oxi hóa
Axit sunfuric đặc háp thụ mạnh nước. Axit sunfuric đặc chiếm các nguyên tử H và O là những nguyên tố thành phần của các hợp chất gluxit giải phóng cacbon và nước.
C12H22O11 → 12C + 11H2O.
Da thịt tiếp xúc với H2SO4 đặc sẽ bị bỏng rất nặng, vì vậy khi sử dụng axit sunfuric phải hết sức thận trọng
Đúng 0
Bình luận (0)
a) Dung dịch axit sunfuric loãng có những tính chất chung của axit, đó là:
- Đổi màu quỳ tím thành đỏ.
- Tác dụng với kim loại giải phóng hiđro.
Fe + H2SO4 \(\rightarrow\) FeSO4 + H2
- Tác dụng với oxit bazơ và bazơ
Ba(OH)2 + H2SO4 \(\rightarrow\) BaSO4 + 2H2O
- Tính chất với nhiều chất muối
BaCl2 + H2SO4 \(\rightarrow\) BaSO4 +2HCl
b) Tính chất hóa học đặc trưng của axit sunfuric đặc là tính oxi hóa mạnh và tính háo nước.
- Tính chất oxi hóa mạnh
2H2SO4 + Cu \(\rightarrow\) CuSO4 + SO2 + 2H2O
2H2SO4 + S \(\rightarrow\) 3SO2 + 2H2O
2H2SO4 + 2KBr \(\rightarrow\) Br2 + SO2 + 2H2O + K2SO4
- Tính háo nước và tính chất oxi hóa
Axit sunfuric đặc háp thụ mạnh nước. Axit sunfuric đặc chiếm các nguyên tử H và O là những nguyên tố thành phần của các hợp chất gluxit giải phóng cacbon và nước.
C12H22O11 \(\rightarrow\) 12C + 11H2O.
Da thịt tiếp xúc với H2SO4 đặc sẽ bị bỏng rất nặng, vì vậy khi sử dụng axit sunfuric phải hết sức thận trọng.
Đúng 0
Bình luận (0)
Bài 1: Trình bày tính chất hóa học của nước? Mỗi tính chất viết một phương trình hóa học minh họa?
-- GIÚP ---- CCaanf gấp
b. Tính chất hóa học của nước
- Tác dụng với kim loại: nước có thể tác dụng với một số kim loại ở nhiệt độ thường như Ca, Ba, K,…
PTHH: K + H2O → KOH + H2
- Tác dụng với mốt sô oxit bazo như CaO, K2O,… tạo ra bazo tương ứng Ca(OH)2, KOH,…
- Dung dịch bazơ làm quỳ tím chuyển xanh
VD: K2O + H2O → 2KOH
- Tác dụng với oxit axit như SO3, P2O5,… tạo thành axit tương ứng H2SO4, H3PO4,…
- Dung dịch axit làm quỳ tím chuyển đỏ
VD: SO3 + H2O → H2SO4
Đúng 0
Bình luận (1)
-Tác dụng với một số oxit axit tạo thành axit
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
-Tác dụng với một số oxit bazơ tạo hành bazơ
\(Na_2O+H_2O\rightarrow2NaOH\)
-Tác dụng với một số kim loại ở nhiệt độ thường tạo thành bazơ và khí H2
\(2K+2H_2O\rightarrow2KOH+H_2\)
Đúng 0
Bình luận (1)
Hãy cho biết những tính chất hóa học đặc trưng của:
Hiđro sunfua.
Dẫn ra những phản ứng hóa học để minh họa.
Tính chất hóa học của hiđro sunfua.
- Hidro sunfua tan trong nước thành dung dịch axit rất yếu.
- Tính khử mạnh :
2H2S + O2 → 2S ↓ + 2H2O
2H2S + 3O2 → 2SO2 + 2H2O
Đúng 0
Bình luận (0)



















